Фармакологические группы:
Химическое название
Фармакология
Фармакодинамика
Как и природные пептидные гормоны соматостатин-14 и соматостатин-28 (подавляют секрецию гормона роста), пасиреотид оказывает фармакологическое действие, связываясь с рецепторами соматостатина. Известно пять разных подтипов человеческого рецептора к соматостатину (SSTR - human somatostatin receptor): SSTR 1, 2, 3, 4 и 5. Пасиреотид с высокой аффинностью связывается с четырьмя из пяти SSTR-рецепторов.
Рецепторы к соматостатину экспрессируются во многих тканях, в особенности в нейроэндокринных опухолях, которые секретируют избыток гормонов, в т.ч. АКТГ, при болезни Иценко-Кушинга. Благодаря способности прочно связываться с рецепторами соматостатина, пасиреотид может применяться для лечения заболеваний, которые характеризуются экспрессией данных рецепторов в тканях-мишенях.
Исследования in vitro показали, что клетки АКТГ-продуцирующей опухоли гипофиза, удаленной у пациентов с болезнью Иценко-Кушинга, экспрессируют большое количество SSTR 5, в то время как другие подтипы рецепторов либо не экспрессируются вообще, либо экспрессируются в меньшем количестве. Пасиреотид связывается с SSTR-рецепторами клеток АКТГ-продуцирующих аденом гипофиза, что приводит к ингибированию секреции АКТГ. Высокое сродство к 4 из 5 подтипов рецепторов соматостатина, в особенности к SSTR 5, обусловливает возможность применения пасиреотида для эффективного лечения пациентов с болезнью Иценко-Кушинга.
В клинических исследованиях пасиреотид уже через 1 мес показал снижение средней суточной концентрации кортизола в моче, и этот эффект сохранялся с течением времени. Отмечалось снижение сАД и дАД, ИМТ и концентрации общего Хс. Кроме того, на фоне лечения отмечено уменьшение клинической симптоматики: гиперемии лица, количества подключичной жировой клетчатки и жировой клетчатки в области спины.
Метаболизм глюкозы
При применении пасериотида в дозе 0,6 и 0,9 мг 2 раза в сутки у здоровых добровольцев было отмечено развитие гипергликемии со значительным снижением секреции инсулина и инкретиновых гормонов (например ГПП-1 и ГИП). Пасиреотид не влиял на чувствительность тканей к инсулину. В другом исследовании у здоровых добровольцев влияние пасиреотида на концентрацию глюкозы в крови изучали, сравнивая группы участников исследования, получавших пасиреотид в монотерапии или в комбинации с гипогликемическим ЛС (метформин, натеглинид, вилдаглиптин или лираглутид соответственно; препараты инсулина не были включены в исследование) на протяжении 7 дней. Гипогликемические ЛС из группы агонистов рецепторов ГПП-1 и ингибиторов ДПП-4 были наиболее эффективны для лечения гипергликемии, ассоциированной с применением пасиреотида.
Влияние на электрофизиологию сердца
Эффект пасиреотида на длину интервала QT оценивали в двух открытых контролируемых перекрестных исследованиях. Было показано, что пасиреотид влияет на интервал QTc, причем максимальное изменение средней длины этого интервала относительно исходного значения (после вычитания эффекта плацебо) наблюдалось через 2 ч после введения пасиреотида. На фоне применения пасиреотида наблюдалось снижение ЧСС; в случае применения пасиреотида в дозе 0,6 мг 2 раза в сутки максимальная разница по сравнению с плацебо наблюдалась через 1 ч (−10,39 мин−1), а в случае применения пасиреотида в дозе 1,95 мг 2 раза в сутки — через 0,5 ч (−14,91 мин−1). Преходящих или продолжительных эпизодов пируэтной тахикардии отмечено не было.
Удлинение интервала QT при применении пасериотида не опосредовано влиянием препарата на калиевые каналы сердца человека, кодируемые геном hERG (human ether-a-go-go-related gene). Эффект пасиреотида на процесс восстановления сердца оценивался при 24-часовом ЭКГ-мониторинге с целью определения его способности увеличивать риск возникновения аритмии.
Отмечено существенное улучшение параметров восстановления сердца при применении пасиреотида на фоне существующего удлинения интервала QT, что указывает на то, что обусловленное применением пасиреотида удлинение интервала QT не ассоциировано с риском развития аритмии. Количественный анализ морфологических параметров Т-зубца не выявил изменений, указывающих на нарушение пространственной однородности процесса реполяризации сердца.
Фармакокинетика
Всасывание
У здоровых добровольцев пасиреотид быстро всасывается после подкожного введения, и Tmax в плазме крови составляет 0,25–0,5 ч. Cmax и AUC приблизительно соответствуют дозе после однократного и многократного введения. Исследования по оценке биодоступности пасиреотида у человека не проводились.
Распределение
У здоровых добровольцев пасиреотид показывает большой кажущийся объем распределения (Vz/F>100 л). Распределение между кровью и плазмой не зависит от концентрации, пасиреотид преимущественно распределяется в плазме (91%). Пасиреотид умеренно связывается с белками плазмы (88%), причем связывание не зависит от концентрации.
Пасиреотид обладает низкой пассивной проникающей способностью, и вероятнее всего, является субстратом P-gp. Ожидается, что влияние P-gp на всасывание, распределение, метаболизм и экскрецию пасиреотида невелико. Пасиреотид не является субстратом BCRP, ОСТ1 (транспортера органических катионов 1) или ОАТР (органических полипептидов — транспортеров анионов) 1В1, 1В3, 2В1.
Метаболизм
Пасиреотид практически не метаболизируется в печени и почках. У здоровых добровольцев пасиреотид обнаруживается в плазме, моче и кале в основном в неизмененном виде.
Выведение
Пасиреотид выводится главным образом через кишечник и в небольших количествах почками. Было показано, что (55,9±6,63)% радиоактивной дозы выводится в первые 10 дней после приема, в т.ч. (48,3±8,16)% — через кишечник и (7,63±2,03)% — почками. Клиренс (CL/F) пасиреотида у здоровых добровольцев и пациентов с болезнью Иценко-Кушинга составляет приблизительно 7,6 и 3,8 л/ч соответственно.
При многократном п/к введении пасиреотид демонстрирует линейную дозозависимую фармакокинетику в диапазоне доз от 0,05 до 0,6 мг 1 раз в день у здоровых добровольцев и 0,3–1,2 мг 2 раза в день у пациентов с болезнью Иценко-Кушинга. Рассчитанный эффективный Т1/2 у здоровых добровольцев составляет около 12 ч (в среднем от 10 до 13 ч для доз 0,05, 0,2 и 0,6 мг в день).
Популяционный анализ показал, что половая и расовая принадлежность не влияют на фармакокинетические параметры пасиреотида.
Особые категории пациентов
Пациенты в возрасте <18 лет. Эффективность и безопасность пасиреотида у пациентов <18 лет не установлена.
Пациенты >65 лет. Данные анализа применения пасиреотида у пациентов с болезнью Иценко-Кушинга >65 лет дают основания полагать, что безопасность и эффективность его применения в данной популяции существенно не отличаются от применения у пациентов более молодого возраста.
Нарушение функции почек. В данной группе пациентов отдельных клинических исследований не проводилось. Однако, т.к. в выведении пасиреотида у человека почечный клиренс существенной роли не играет, значительное влияние функции почек на концентрацию пасиреотида в крови представляется маловероятным.
Нарушение функции печени. По данным клинического исследования, у пациентов с нарушением функции печени (классы А, В и С по классификации Чайлд-Пью) при применении пасиреотида фармакокинетические показатели были заметно выше, чем у пациентов с нормальной функцией печени: показатель AUCinf повышался на 60 и 79%, Сmax — на 67 и 69%, a CL/F снижался на 37 и 44% соответственно.
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.
Применение пасиреотида при беременности не изучалось. В исследованиях на животных показано, что пасиреотид может оказывать токсическое действие на репродуктивную функцию. Потенциальный риск для человека неизвестен. Пасиреотид следует применять при беременности лишь в крайних случаях, если потенциальная польза превышает возможный риск.
В исследованиях пасиреотида у животных при его п/к введении показано, что он проникает в молоко лактирующих животных.
Неизвестно, проникает ли пасиреотид в грудное молоко у человека. Поскольку риск для ребенка, получающего пасиреотид с грудным молоком, исключить нельзя, в период грудного вскармливания применение пасиреотида противопоказано.
Характеристика
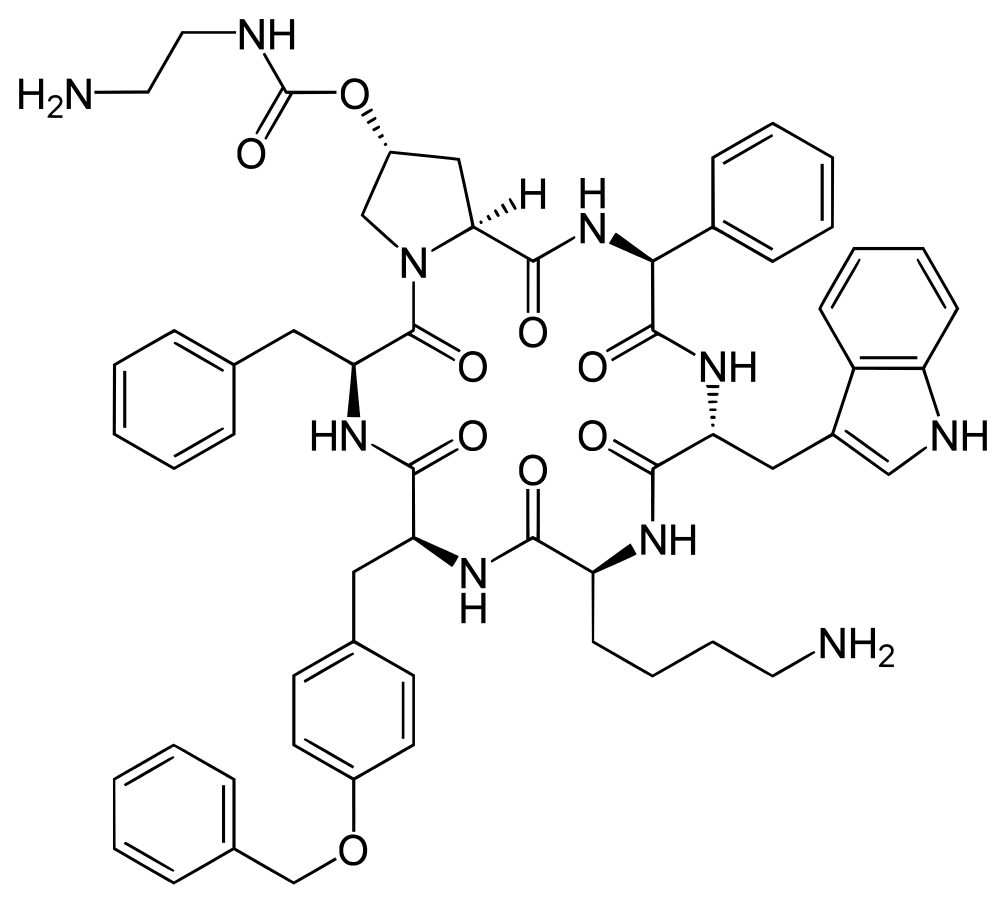
Синтетический аналог соматостатина для инъекционного применения, представляющий собой циклогексапептид..
Применение
Лечение пациентов с болезнью Иценко-Кушинга при невозможности проведения или неэффективности хирургического лечения.
Категория действия на плод по FDA — C.
Применение пасиреотида при беременности не изучалось. В исследованиях на животных показано, что пасиреотид может оказывать токсическое действие на репродуктивную функцию. Потенциальный риск для человека неизвестен. Пасиреотид следует применять при беременности лишь в крайних случаях, если потенциальная польза превышает возможный риск.
В исследованиях пасиреотида у животных при его п/к введении показано, что он проникает в молоко лактирующих животных.
Неизвестно, проникает ли пасиреотид в грудное молоко у человека. Поскольку риск для ребенка, получающего пасиреотид с грудным молоком, исключить нельзя, в период грудного вскармливания применение пасиреотида противопоказано.
Ограничения к применению
Нарушение толерантности к глюкозе или сахарный диабет; заболевания сердца и/или факторы риска развития брадикардии (клинически значимая брадикардия или острый инфаркт миокарда в анамнезе, AV-блокада высокой степени, ХСН (III или IV класс по классификации NYHA), нестабильная стенокардия, стойкая желудочковая тахикардия, фибрилляция желудочков, врожденный синдром удлинения интервала QT); одновременное применение антиаритмических или других ЛС, ведущих к удлинению интервала QT; гипокалиемия и/или гипомагниемия; нарушение функции печени; беременность.
Противопоказания
Повышенная чувствительность к пасиреотиду; тяжелое нарушение функции печени (класс С по Чайлд-Пью); возраст до 18 лет; период грудного вскармливания.
Побочные действия
В клинических исследованиях II и III фазы пасиреотид получал 201 пациент с болезнью Иценко-Кушинга. За исключением случаев развития гипокортицизма и более тяжелой степени гипергликемии, профиль безопасности пасиреотида существенно не отличается от других аналогов соматостатина.
Большинство нежелательных явлений степени тяжести 3 и 4 были связаны с гипергликемией. Наиболее частыми (частота >10%) были диарея, тошнота, боль в животе, холелитиаз, гипергликемия, сахарный диабет, утомляемость и повышение концентрации гликозилированного гемоглобина (HbA1c). Летальных исходов в ходе исследования не было.
Частота развития нежелательных явлений оценивалась следующим образом: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000).
Со стороны крови и лимфатической системы: нечасто — анемия.
Со стороны эндокринной системы: часто — надпочечниковая недостаточность.
Со стороны обмена веществ и нарушение питания: очень часто — гипергликемия, сахарный диабет; часто — сахарный диабет типа 2, снижение аппетита.
Со стороны сердца: часто — синусовая брадикардия, удлинение интервала QT.
Со стороны сосудов: часто — артериальная гипотония.
Со стороны нервной системы: часто — головная боль.
Со стороны пищеварительной системы: очень часто — диарея, боль в животе, тошнота; часто — рвота, боль в верхних отделах живота.
Со стороны печени и желчевыводящих путей: очень часто — холелитиаз.
Со стороны кожи и подкожных тканей: часто — алопеция, зуд.
Со стороны скелетно-мышечной и соединительной ткани: часто — миалгия, артралгия.
Общие расстройства и нарушения в месте введения: очень часто — реакция в месте введения, повышенная утомляемость.
Лабораторные и инструментальные данные: очень часто — повышение HbA1c; часто — повышение концентрации глюкозы в крови, повышение активности липазы, амилазы, гамма-глутамилтрансферазы, AЛT.
Описание отдельных нежелательных явлений
Нарушение метаболизма глюкозы. В исследовании III фазы у пациентов с болезнью Иценко-Кушинга повышение концентрации глюкозы в плазме крови было наиболее частым лабораторным нарушением степени тяжести 3 (23,2% пациентов). У пациентов с нормогликемией на момент включения в исследование средний показатель HbA1c увеличивался в меньшей степени, чем у пациентов с нарушением толерантности к глюкозе или сахарным диабетом.
В течение первого месяца лечения средние показатели концентрации глюкозы плазмы крови натощак обычно увеличивались, а в последующие месяцы снижались и стабилизировались. В течение 28 дней после отмены пасиреотида показатели концентрации глюкозы плазмы крови натощак и HbA1c, как правило, снижались, но оставались выше исходных значений. Данные длительного наблюдения отсутствуют. В ходе клинических исследований по причине развития гипергликемии препарат был отменен у 3,1% пациентов, по причине развития сахарного диабета — у 2,5%.
Расстройства со стороны ЖКТ. Как и в случае других аналогов соматостатина, на фоне применения пасиреотида часто отмечались желудочно-кишечные расстройства. Обычно подобные явления характеризовались низкой степенью выраженности, не требовали вмешательства и разрешались на фоне продолжающегося лечения.
Реакции в месте введения. В клинических исследованиях у 13,6% пациентов отмечались реакции в месте введения пасиреотида, среди них: боль в месте инъекции, эритема, гематома, кровоизлияние и зуд. Данные явления разрешались самопроизвольно и не требовали вмешательства.
Активность ферментов печени. На фоне применения пасиреотида, также как и на фоне применения других аналогов соматостатина отмечалось преходящее повышение активности ферментов печени. В большинстве случаев данные явления не сопровождались клинической симптоматикой, характеризовались низкой степенью выраженности и разрешались, несмотря на продолжение лечения. Было выявлено несколько случаев повышения активности AЛT (в 3 раза выше ВГН) и билирубина (в 2 раза выше ВГН), которые возникали в течение первых 10 дней после начала применения пасиреотида и разрешались на фоне прекращения лечения. Случаев лекарственного гепатита отмечено не было.
Активность ферментов поджелудочной железы. В клинических исследованиях на фоне приема пасиреотида отмечалось повышение активности липазы и амилазы, не сопровождавшееся клинической симптоматикой. Данные явления характеризовались низкой степенью выраженности и разрешались на фоне продолжения лечения. Тем не менее, развитие панкреатита следует считать возможной побочной реакцией аналогов соматостатина, т.к. желчнокаменная болезнь может быть ассоциирована с развитием острого панкреатита.
Следующие клинически значимые побочные реакции упоминаются в других разделах описания:
- гипокортицизм (см. «Меры предосторожности»);
- гипергликемия и диабет (см. «Меры предосторожности»);
- брадикардия и удлинение интервала QT (см. «Меры предосторожности»);
- повышение показателей печеночных тестов (см. «Меры предосторожности»);
- холелитиаз (см. «Меры предосторожности»);
- недостаточность гормонов гипофиза (см. «Меры предосторожности»).
Опыт клинических испытаний
Так как клинические испытания проводились с различным набором условий, частота встречаемости побочных реакций, наблюдавшихся в этих исследованиях, может не совпадать с полученной в других исследованиях и наблюдаемой в клинической практике.
В общей сложности 162 пациента с болезнью Иценко-Кушинга получали пасиреотид в клинических исследованиях III фазы. В начале исследования пациенты были рандомизированы по двум группам, получавшим пасиреотид п/к 2 раза в день в дозе 0,6 или 0,9 мг. Средний возраст пациентов составил приблизительно 40 лет, число пациентов женского пола превалировало (78%). Основная часть пациентов имела персистирующую или рецидивирующую форму болезни Иценко-Кушинга (83%); некоторые пациенты (≤5%) в каждой из исследуемых групп получали предшествующее облучение гипоталамогипофизарной системы. Средняя экспозиция пасиреотида составила 10,4 мес, 68% пациентов получали пасиреотид по крайней мере 6 мес. В III фазе клинического иследования побочные реакции были отмечены у 98% пациентов. Наиболее часто (с частотой ≥20% в каждой группе) отмечались диарея, тошнота, гипергликемия, холелитиаз, головная боль, абдоминальная боль, повышенная утомляемость и сахарный диабет. Смертельные случаи в ходе данного исследования не отмечены. Серьезные побочные реакции наблюдались у 25% пациентов. У 17% пациентов отмечены побочные реакции, приведшие к прекращению исследования.
Ниже перечислены побочные реакции, наблюдавшиеся с общей частотой более 5% в рандомизированных группах и в исследовании в целом. Побочные реакции ранжированы по частоте встречаемости, наиболее часто наблюдавшиеся побочные реакции приведены первыми. Данные представлены через точку с запятой в следующем порядке (число случаев (доля от числа участников, %): группа получавших пасиреотид в дозе 0,6 мг 2 раза в день (N=82); группа получавших пасиреотид в дозе 0,9 мг 2 раза в день (N=80); в целом по обеим группам (N=162).
Диарея — 48 (59%); 46 (58%); 94 (58%).
Тошнота — 38 (46%); 46 (58%); 84 (52%).
Гипергликемия — 31 (38%); 34 (43%); 65 (40%).
Холелитиаз — 25 (30%); 24 (30%); 49 (30%).
Головная боль — 23 (28%); 23 (29%); 46 (28%).
Абдоминальная боль — 19 (23%); 20 (25%); 39 (24%).
Повышенная утомляемость — 12 (15%); 19 (24%); 31 (19%).
Сахарный диабет — 13 (16%); 16 (20%); 29 (18%).
Реакции в месте введения — 14 (17%); 14 (18%); 28 (17%).
Назофарингит — 10 (12%); 11 (14%); 21 (13%).
Алопеция — 10 (12%); 10 (13%); 20 (12%).
Астения — 13 (16%); 5 (6%); 18 (11%).
Увеличение уровня HbA1c — 10 (12%); 8 (10%); 18 (11%).
Увеличение уровня АЛТ — 11 (13%); 6 (8%); 17 (10%).
Увеличение уровня гамма-глутамил трансферазы — 10 (12%); 7 (20%); 17 (10%).
Периферический отек — 9 (11%); 8 (10%); 17 (10%).
Боль в верхней части живота — 10 (12%); 6 (8%); 16 (10%).
Понижение аппетита — 7 (9%); 9 (11%); 16 (10%).
Гиперхолестеринемия — 7 (9%); 9 (11%); 16 (10%).
Гипертензия — 8 (10%); 8 (10%); 16 (10%).
Головокружение — 8 (10%); 7 (9%); 15 (9%).
Гипогликемия — 12 (15%); 3 (4%); 15 (9%).
Сахарный диабет типа 2 — 10 (12%); 5 (6%); 15 (9%).
Беспокойство — 5 (6%); 9 (11%); 14 (9%).
Грипп — 9 (11%); 5 (6%); 14 (9%).
Бессонница — 3 (4%); 11 (14%); 14 (9%).
Миалгия — 10 (12%); 4 (5%); 14 (9%).
Артралгия — 5 (6%); 8 (10%); 13 (8%).
Зуд — 6 (7%); 7 (9%); 13 (8%).
Увеличение уровня липазы — 7 (9%); 5 (6%); 12 (7%).
Запор — 7 (9%); 4 (5%); 11 (7%).
Гипотензия — 5 (6%); 6 (8%); 11 (7%).
Рвота — 3 (4%); 8 (10%); 11 (7%).
Боль в спине — 4 (5%); 6 (8%); 10 (6%).
Сухость кожи — 5 (6%); 5 (6%); 10 (6%).
Удлинение интервала QT на ЭКГ — 5 (6%); 5 (6%); 10 (6%).
Гипокалиемия — 6 (7%); 4 (5%); 10 (6%).
Боль в конечностях — 6 (7%); 4 (5%); 10 (6%).
Синусовая брадикардия — 8 (10%); 2 (3%); 10 (6%).
Вертиго — 4 (5%); 6 (8%); 10 (6%).
Вздутие живота — 4 (5%); 5 (6%); 9 (6%).
Надпочечниковая недостаточность — 4 (5%); 5 (6%); 9 (6%).
Увеличение уровня АСТ — 6 (7%); 3 (4%); 9 (6%).
Увеличение уровня глюкозы в крови — 6 (7%); 3 (4%); 9 (6%).
Другими значимыми побочными реакциями, возникавшими с частотой менее 5%, были анемия (4%), повышение уровня амилазы в крови (2%) и увеличение ПВ (2%).
Нарушения со стороны ЖКТ
В исследовании III фазы часто сообщалось о нарушениях со стороны ЖКТ, преимущественно в виде диареи, тошноты, абдоминальной боли и рвоты. Такие побочные реакции начинали развиваться главным образом в первый месяц лечения пасиреотидом и не требовали вмешательства.
Гипергликемия и диабет
В исследовании III фазы часто сообщалось о побочных реакциях, связанных с гипергликемией. Для всех пациентов такие реакции включали гипергликемию (40%), сахарный диабет (18%), увеличение уровня HbA1c (11%) и сахарный диабет типа 2 (9%). В основном увеличение уровня глюкозы в плазме крови натощак и HbA1c наблюдалось вскоре после начала лечения пасиреотидом и сохранялось в ходе лечения. В группе пациентов, получавших пасиреотид в дозе 0,6 мг, средний уровень глюкозы в плазме крови натощак увеличился с 98,6 мг/дл (исходный уровень) до 125,1 мг/дл на 6-й месяц лечения. В группе получавших пасиреотид в дозе 0,9 мг увеличение от исходного уровня в 97 мг/дл составило до 128 мг/дл на 6-й месяц. Аналогичное увеличение уровня HbA1c в указанных группах составило от 5,8 до 7,2% и от 5,8 до 7,3% соответственно (см. «Меры предосторожности»).
За один месяц после отмены пасиреотида средние уровни глюкозы в плазме крови натощак и HbA1c уменьшались, но оставались выше исходного уровня. Данные более длительного наблюдения недоступны.
Повышение показателей печеночных тестов
В исследовании III фазы у пациентов, получавших пасиреотид, наблюдалось транзиторное повышение средних значений уровня аминотрансферазы. Средние значения возвращались к исходному уровню к 4-му месяцу лечения. Данные повышения не были связаны с клиническими симптомами заболевания печени.
В программе клинических исследований пасиреотида у 4 пациентов наблюдалось параллельное повышение уровня АЛТ >3×ВГН и билирубина >2×ВГН, 1 пациент был с болезнью Иценко-Кушинга и 3 — здоровые добровольцы (см. «Меры предосторожности»). Во всех четырех случаях эти повышения не были замечены в первые 10 дней лечения. Во всех этих случаях повышения уровня общего билирубина сопутствовали или предшествовали повышению уровня трансаминазы. У пациента с болезнью Иценко-Кушинга развилась желтуха. При отмене пасиреотида отклонения лабораторных показателей разрешились во всех четырех случаях.
Гипокортицизм
В исследованиях III фазы у пациентов с болезнью Иценко-Кушинга были отмечены случаи гипокортицизма (см. «Побочные действия»). Большинство этих случаев разрешалось уменьшением дозы пасиреотида и/или добавлением краткосрочной терапии ГКС в низких дозах (см. «Меры предосторожности»).
Реакции в месте введения
Реакции в месте введения наблюдались у 17% пациентов, участвовавших в исследовании III фазы по применению пасиреотида при болезни Иценко-Кушинга. Такие случаи чаще всего отмечались как боль в месте введения, эритема, гематома, геморрагия и зуд. Эти случаи разрешались спонтанно и не требовали вмешательства.
Функция щитовидной железы
У 7 пациентов, принимавших участие в исследовании III фазы по изучению применения пасиреотида при болезни Иценко-Кушинга, были отмечены случаи гипотиреоидизма. Все 7 пациентов имели в начале исследования уровень ТТГ близкий к НГН или меньше, что исключает возможность установить убедительную связь между этим побочным явлением и применением пасиреотида.
Другие отклонения лабораторных показателей
У пациентов, получавших пасиреотид в клинических исследованиях, наблюдалось асимптоматическое и обратимое повышение уровня липазы и амилазы. Панкреатит является потенциальной побочной реакцией, связанной с применением аналогов соматостатина, из-за связи между холелитиазом и острым панкреатитом.
Наблюдалось незначительное увеличение уровня Hb, которое оставалось в пределах нормы. Также отмечено повышение уровня ПВ и частичного тромбопластинового времени по сравнению с исходным уровнем у 33 и 47% пациентов соответственно. Эти повышения были минимальными.
Данные лабораторные отклонения не представляют клинической значимости.
Взаимодействие
Пасиреотид в умеренной степени связывается с белками плазмы, лишь в небольшой степени подвергается метаболизму. Пасиреотид является субстратом P-gp, но не ингибитором или индуктором P-gp. Нет данных, позволяющих предполагать, что в терапевтических концентрациях пасиреотид является:
- субстратом, ингибитором или индуктором цитохрома Р450;
- субстратом BCRP, ОСТ1 или ОАТР1В1, 1ВЗ, 2В1;
- ингибитором УДФ-ГТ1A1, белков-переносчиков ОАТ1 или ОАТЗ, ОАТР1В1 или 1ВЗ, ОСТ1 или ОСТ2, P-gp, BCRP, белка-переносчика MRP2 или ВSEP (экспортирующей помпы желчных кислот).
В исследовании влияния ингибитора P-gp на фармакокинетику пасиреотида, при его п/к введении одновременно с применением верапамила, у здоровых добровольцев не отмечено изменение показателей биодоступности пасиреотида.
Фармакокинетические взаимодействия, влияющие на эффект пасиреотида. Существует риск увеличения Сmах пасиреотида при одновременном применении с ингибиторами P-gp (кетоконазол, циклоспорин, верапамил, кларитромицин), клинического подтверждения данного эффекта нет.
Фармакокинетические взаимодействия, влияющие на эффект сопутствующих ЛС. Немногочисленные опубликованные данные свидетельствуют о том, что аналоги соматостатина опосредованно (через подавление секреции СТГ) могут снижать клиренс веществ, метаболизирующихся при участии изоферментов цитохрома Р450. Имеющиеся данные не позволяют исключить подобный эффект и у пасиреотида. Пасиреотид следует с осторожностью применять одновременно с ЛС, имеющими узкий терапевтический индекс и метаболизирующимися преимущественно при участии изофермента CYP3A4 (хинидин, терфенадин).
В исследовании на собаках показано, что пасиреотид снижает концентрацию циклоспорина в крови за счет уменьшения всасывания последнего в кишечнике. Имеет ли место подобное взаимодействие у человека, неизвестно. В этой связи, в случае применения пасиреотида одновременно с циклоспорином может возникнуть необходимость в коррекции дозы циклоспорина.
Немногочисленные данные для других аналогов соматостатина позволяют предположить, что в случае применения пасиреотида одновременно с бромокриптином биодоступность последнего увеличивается.
Лекарственные средства, влияющие на интервал QT. Пасиреотид следует с осторожностью применять одновременно с антиаритмическими и другими ЛС, способными удлинять интервал QT: антиаритмические ЛС (хинидин, прокаинамид, дизопирамид, амиодарон, дронедарон, соталол, дофетилид, ибутилид), отдельные антибактериальные ЛС (эритромицин для в/в применения, кларитромицин, моксифлоксацин), отдельные антипсихотические ЛС (хлорпромазин, тиоридазин, флуфеназин, галоперидол, тиаприд, амисульприд, сертиндол, метадон), некоторые блокаторы Н1-гистаминовых рецепторов (терфенадин, астемизол, мизоластин), противомалярийные ЛС (хлорохин, галофантрин, лумефантрин), некоторые противогрибковые ЛС (кетоконазол).
Рекомендуется также контролировать ЧСС у пациентов, принимающих одновременно пасиреотид и ЛС, вызывающие брадикардию: бета-адреноблокаторы (метопролол, пропранолол, соталол), м-холиноблокаторы (ипратропия бромид, оксибутинин), БКК (верапамил, дилтиазем, бепридил) и антиаритмические ЛС.
Инсулин и пероральные гипогликемические ЛС. Пациентам, получающим инсулин или пероральные гипогликемические ЛС, может потребоваться коррекция дозы (увеличение или уменьшение) данных ЛС после начала лечения пасиреотидом.
Влияние других ЛС на пасиреотид
ЛС, пролонгирующие интервал QT. Совместное применение ЛС, пролонгирующих интервал QT, и пасиреотида может оказать аддитивный эффект на пролонгацию интервала QT. Следует соблюдать осторожность при совместном применении пасиреотида и ЛС, пролонгирующих интервал QT (см. «Меры предосторожности»).
Влияние пасиреотида на другие ЛС
Циклоспорин. Совместное применение циклоспорина и пасиреотида может уменьшить относительную биодоступность циклоспорина, и вследствие этого может потребоваться коррекция дозы циклоспорина для поддержания его терапевтического уровня.
Бромокриптин. Совместное применение аналогов соматостатина и бромокриптина может увеличить уровень бромокриптина в крови. Может потребоваться уменьшение дозы бромокриптина.
Пути введения
П/к.
Меры предосторожности
Гипокортицизм
Лечение пасиреотидом приводит к быстрому снижению секреции АКТГ у пациентов с болезнью Иценко-Кушинга. Быстрая и полная или почти полная супрессия секреции АКТГ может приводить к снижению концентрации кортизола плазмы крови и развитию преходящего гипокортицизма. Случаи гипокортицизма были описаны у пациентов с болезнью Иценко-Кушинга в исследованиях III фазы; гипокортицизм развивался как правило в первые 2 мес лечения. В большинстве случаев данное состояние купировалось за счет снижения дозы пасиреотида и/или добавления краткосрочной терапии небольшими дозами ГКС.
Необходимо контролировать состояние и инструктировать пациентов относительно возможного возникновения симптомов гипокортицизма (например слабость, повышенная утомляемость, тошнота, рвота, артериальная гипотензия, гипонатриемия или гипогликемия). В случае подтвержденного гипокортицизма может потребоваться временная заместительная терапия ГКС и/или снижение дозы пасиреотида, или перерыв в лечении.
Гипокортицизм
Лечение пасиреотидом ведет к подавлению секреции АКТГ при болезни Иценко-Кушинга. Подавление секреции АКТГ может привести к снижению уровня циркулирующего кортизола и потенциально — к гипокортицизму.
Следует осуществлять контроль и инструктировать пациента о признаках и симптомах, связанных с гипокортицизмом (например слабость, повышенная утомляемость, анорексия, тошнота, рвота, гипотензия, гипонатриемия или гипогликемия). При проявлениях гипокортицизма следует рассмотреть временное уменьшение дозы или перерыв в лечении пасиреотидом, а также временную заместительную терапию ГКС.
Метаболизм глюкозы
У пациентов, получающих пасиреотид, возможно развитие гипергликемии (реже гипогликемии).
Развитие гипергликемии, по-видимому, связано с уменьшением секреции инсулина (особенно в промежутке времени после введения пасиреотида) и инкретиновых гормонов (например ГПП-1 и ГИП).
Гипергликемия сильнее выражена у пациентов, имевших до начала терапии нарушение толерантности к глюкозе или сахарный диабет. До начала применения пасиреотида следует оценить концентрацию глюкозы крови натощак и HbA1c. В течение первых 2–3 мес лечения пациенты должны самостоятельно контролировать концентрацию глюкозы в крови (натощак) с интервалами в 1 нед, а также в первые 2–4 нед после увеличения дозы пасиреотида; впоследствии эти показатели необходимо контролировать по мере клинической необходимости.
Если на фоне применения пасиреотида у пациента развивается гипергликемия, рекомендовано применение гипогликемических средств или коррекция схемы их применения.
При лечении гипогликемическими ЛС отмечалось снижение концентрации HbA1c <7% и глюкозы крови натощак <130 мг/дл (7,2 ммоль/л) у 43 и 72% пациентов с болезнью Иценко-Кушинга соответственно. При стойкой гипергликемии, плохо поддающейся коррекции при адекватной гипогликемической терапии, требуется снижение дозы пасиреотида или его отмена. У пациентов с болезнью Иценко-Кушинга и гипергликемией, плохо поддающейся коррекции (HbA1c >8% на фоне терапии гипогликемическими ЛС), повышен риск развития тяжелой гипергликемии и связанных с ней осложнений (например кетоацидоз). У пациентов с гипергликемией, плохо поддающейся коррекции, перед началом применения пасиреотида следует усилить гликемический контроль и скорректировать терапию сахарного диабета.
Гипергликемия и диабет
У здоровых добровольцев и пациентов, получавших пасиреотид, наблюдалось повышение уровня глюкозы в крови. В исследовании III фазы отмечалось развитие предиабета и диабета. В этом исследовании почти у всех пациентов, включая имевших нормальный исходный уровень глюкозы, предиабет и диабет, в первые 2 нед лечения развивалась гипергликемия. Пациенты с болезнью Иценко-Кушинга и плохо поддающейся контролю гликемией (определяется по значению HbA1c >8% на фоне противодиабетической терапии) могут быть подвержены более высокому риску развития тяжелой гипергликемии и связанных с ней осложнений, например кетоацидоза.
В связи с предсказуемостью данной побочной реакции, перед началом лечения пасиреотидом необходимо определить гликемический статус (уровень глюкозы в плазме крови натощак или HbA1c). У пациентов с неконтролируемым сахарным диабетом перед началом лечения пасиреотидом необходимо начать интенсивную противодиабетическую терапию. Самостоятельный контроль уровня глюкозы в крови и/или определение уровня глюкозы в плазме крови натощак необходимо проводить каждую неделю в течение первых 2–3 мес лечения и впоследствии периодически, при клинической необходимости. После отмены лечения гликемический мониторинг (например уровень глюкозы в плазме крови натощак или HbA1c) должен осуществляться в соответствии со сложившей клинической практикой. У пациентов, которым назначена противодиабетическая терапия как результат применения пасиреотида, может потребоваться более тщательный мониторинг после прекращения лечения, в особенности если противодиабетическая терапия связана с риском возникновения гипогликемии.
У пациентов с гипергликемией, развившейся на фоне терапии пасиреотидом, рекомендуется начать или скорректировать противодиабетическую терапию. Оптимальное лечение для контроля гипергликемии, вызванной приемом пасиреотида, неизвестно. Если, несмотря на соответствующее лечение, гипергликемия остается неконтролируемой, следует уменьшить дозу пасиреотида или прекратить его прием.
Нарушения со стороны ССС
На фоне применения пасиреотида отмечались случаи брадикардии. Необходимо тщательное наблюдение за пациентами с заболеванием сердца и/или факторами риска развития брадикардии (в частности у пациентов, в анамнезе которых имеется клинически значимая брадикардия или острый инфаркт миокарда, AV-блокада высокой степени, ХСН (III или IV класс по классификации NYHA), нестабильная стенокардия, стойкая желудочковая тахикардия, фибрилляция желудочков). Может потребоваться коррекция дозы ЛС, таких как бета-адреноблокаторы, антагонисты кальция.
Пасиреотид следует с осторожностью применять у пациентов, у которых интервал QT либо уже удлинен, либо может быть удлинен с высокой вероятностью, в частности у пациентов:
- с врожденным синдромом удлинения интервала QT;
- с неконтролируемым или серьезным заболеванием сердца, в т.ч. недавно перенесенным инфарктом миокарда, ХСН, нестабильной стенокардией или клинически значимой брадикардией;
- принимающих антиаритмические или другие ЛС, ведущие к удлинению интервала QT;
- с гипокалиемией и/или гипомагниемией.
Рекомендуется контролировать длину интервала QTc на фоне применения пасиреотида: ЭКГ-исследование рекомендуется проводить перед началом лечения, а затем по клиническим показаниям. До начала терапии пасиреотидом у пациентов с гипокалиемией и гипомагниемией необходимо нормализовать содержание калия и магния в плазме крови; на фоне дальнейшего лечения следует периодически контролировать их концентрацию.
Брадикардия и удлинение интервала QT
Брадикардия. При применении пасиреотида были отмечены случаи брадикардии (см. «Побочные действия»). Следует установить тщательный контроль у пациентов с сердечными заболеваниями и/или факторами риска развития брадикардии, такими как клинически значимая брадикардия в анамнезе, AV-блокада высокой степени или сопутствующее применение ЛС, ассоциированных с брадикардией. Может потребоваться коррекция дозы бета-адреноблокаторов, БКК или коррекция электролитных нарушений.
Удлинение интервала QT. Применение пасиреотида ассоциируется с удлинением интервала QT. Удлинение интервала QT наблюдалось в двух исследованиях с применением пасиреотида в терапевтических и сверхтерапевтических дозах. Следует соблюдать осторожность при применении пасиреотида у пациентов с факторами повышенного риска развития удлинения интервала QTc, такими как:
- врожденное длительное удлинение интервала QT;
- неконтролируемое или серьезное заболевание сердца, включая недавно перенесенный инфаркт миокарда, ХСН, нестабильную стенокардию или клинически значимую брадикардию;
- терапия антиаритмическими или другими ЛС, с известной способностью удлинять интервал QT;
- гипокалиемия и/или гипомагниемия.
Перед началом применения пасиреотида рекомендуется выполнить ЭКГ, а в ходе лечения — осуществлять наблюдение за влиянием терапии пасиреотидом на интервал QT. Перед назначением пасиреотида необходимо скорректировать гипокалиемию и гипомагниемию и в ходе терапии периодически проверять наличие этих состояний.
Биохимические показатели функции печени
Рекомендуется определять биохимические показатели функции печени (билирубин, активность печеночных ферментов) до начала терапии пасиреотидом, через 1–2 нед терапии, а затем ежемесячно на протяжении 3 мес. Затем биохимические показатели функции печени исследуются по клиническим показаниям. Терапию пасиреотидом следует прекратить в следующих случаях:
- у пациента на фоне приема пасиреотида развилась желтуха или другие признаки выраженного нарушения функции печени;
- активность ACT или AЛT повысилась до значений в 5 раз более ВГН или выше;
- активность АЛТ и ACT достигла уровня в 3 раза выше ВГН и концентрация билирубина достигла значений в 2 раза выше ВГН.
Если нарушение биохимических показателей функции печени предположительно связано с применением пасиреотида, дальнейшее возобновление терапии не рекомендуется.
Повышение показателей печеночных тестов
В исследовании III фазы у 5% пациентов уровень АЛТ или АСТ был >3×ВГН. В целом в ходе выполнения программы клинических исследований пасиреотида отмечено 4 случая сопутствующего повышения уровня АЛТ >3×ВГН и билирубина >2×ВГН — у 1 пациента с болезнью Иценко-Кушинга и 3 у здоровых добровольцев (см. «Побочные действия»). В этих случаях повышение уровня общего билирубина, по-видимому, сопутствовало или предшествовало повышению уровня трансаминазы.
Следует проверять показатели печеночных тестов через 1–2 нед после начала лечения, затем ежемесячно в течение 3 мес и в последующем каждые 6 мес. Если исходный уровень АЛТ нормальный и в ходе лечения наблюдается повышение АЛТ до 3–5×ВГН, следует повторить анализ в течение недели или в течение 48 ч, если превышение составило >5×ВГН. Если исходное значение АЛТ отклоняется от нормы и повышение уровня АЛТ в ходе лечения составляет 3–5×ВГН от исходного уровня, анализ следует повторить в течение недели или раньше, если превышение составляет >5×ВГН. Анализы следует проводить в лаборатории, предоставляющей результаты в тот же день. Если результаты повторного анализа подтверждают первичные результаты или показывают их повышение, необходимо приостановить применение пасиреотида и изучить возможную причину данного явления, которая может быть связана или не связана с применением пасиреотида. При любом превышении исходного уровня в 5 раз при исходном уровне, отличающемся от нормального, и до 5×ВГН при нормальном исходном уровне следует еженедельно или более часто проводить серийные измерения АЛТ, АСТ, ЩФ и общего билирубина. Лечение пасиреотидом может быть возобновлено с осторожностью при возвращении показателей к нормальному или близкому к нормальному уровню при тщательном наблюдении и только, если какая-либо другая возможная причина найдена.
Холелитиаз
Холелитиаз — установленный неблагоприятный побочный эффект, связанный с длительным применением аналогов соматостатина, в т.ч. пасиреотида. Рекомендуется проводить УЗИ желчного пузыря до начала применения пасиреотида и через каждые 6–12 мес его применения. Наличие камней в желчном пузыре у пациентов, получающих пасиреотид, в большинстве случаев не сопровождается клиническими проявлениями. Желчнокаменную болезнь, сопровождающуюся характерной клинической симптоматикой, следует лечить в соответствии с принятой клинической практикой.
Холелитиаз
В клинических исследованиях пасиреотида отмечались частые случаи холелитиаза (см. «Побочные действия»). Рекомендуется проводить УЗИ желчного пузыря перед началом применения пасиреотида и в последующем с интервалом 6–12 мес в ходе лечения.
Гормоны гипофиза
Поскольку по своей фармакологической активности пасиреотид напоминает соматостатин, нельзя исключить, что на фоне его применения будет подавляться синтез не только АКТГ, но и других гипофизарных гормонов. В связи с этим, как перед началом лечения пасиреотидом, так и в ходе лечения (по клиническим показаниям) следует контролировать функцию гипофиза (включая определение концентрации ТТГ, гормона роста), а также свободного тироксина.
Мониторинг недостаточности гормонов гипофиза
Поскольку фармакологическое действие пасиреотида сходно с действием соматостатина, возможно ингибирование других, кроме АКТГ, гормонов гипофиза. Перед назначением пасиреотида и периодически в ходе лечения при клинической необходимости может потребоваться контроль функции гипофиза (например ТТГ/свободный тироксин, гормон роста/ИФР-1). Пациенты после проведения транссфеноидальной хирургии или облучения гипофиза, находятся в группе повышенного риска развития недостаточности гормонов гипофиза.
Влияние на способность управлять транспортными средствами и/или работать с механизмами. Исследования влияния пасиреотида на способность управлять транспортными средствами и работать с механизмами не проводились. Учитывая возможность развития некоторых побочных эффектов (головная боль, повышенная утомляемость), пациентам следует соблюдать осторожность при управлении транспортными средствами и занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания.
Передозировка
У пациентов, получавших пасиреотид п/к, случаев передозировки отмечено не было. У здоровых добровольцев, получавших пасиреотид в дозах до 2,1 мг 2 раза в сутки, в качестве побочного явления часто отмечалась диарея.
В случае передозировки пасиреотида следует, основываясь на состоянии пациента, начать соответствующее симптоматическое лечение и проводить его до разрешения симптомов.