Фармакологические группы:
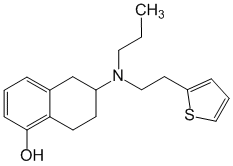
Химическое название
Фармакология
Фармакодинамика
Неэрголиновый агонист D1–3-дофаминовых рецепторов, применяемый для лечения болезни Паркинсона. Терапевтический эффект ротиготина обусловлен активацией D3, D2 и D1-рецепторов каудато-путаменального (базальные ядра — хвостатые и скорлупы) комплекса головного мозга. Ротиготин ослабляет выраженность клинических проявлений идиопатической болезни Паркинсона (ИБП).
Данные клинических исследований
Эффективность ротиготина для лечения пациентов с ИБП подтверждена результатами 4 рандомизированных двойных слепых плацебо-контролируемых исследований.
В двух исследованиях ротиготин назначали пациентам без сопутствующей терапии агонистами дофаминовых рецепторов, которые не получали препараты леводопы или получали их не более 6 мес. Главным критерием оценки эффективности терапии была сумма баллов по II (повседневная активность) и III (двигательная активность) частям Унифицированной шкалы оценки болезни Паркинсона (УШОБП). В обоих исследованиях начальная доза ротиготина составляла 2 мг/24 ч. Эту дозу еженедельно повышали на 2 мг/24 ч до достижения оптимальной, которая оставалась неизменной в течение 6 мес.
В первом двойном слепом исследовании 177 пациентов получали ротиготин и 96 — плацебо. В конце лечения оптимальная доза составила 6 мг/24 ч, у 91% пациентов она совпала с максимальной разрешенной.
Улучшение на 20% наблюдалось у 48% в группе ротиготина и 19% — в группе плацебо, преимущество ротиготина составило 29% (p<0,0001). Улучшение по УШОБП в группе ротиготина составляло 3,98 балла (сумма баллов до лечения — 29,9), тогда как в группе плацебо наблюдалось ухудшение на 1,31 балла (сумма баллов до лечения — 30). Разница между ротиготином и плацебо составила 5,28 балла и являлась статистически значимой (p<0,0001).
Во втором двойном слепом исследовании 213 пациентов получали ротиготин, 227 — ропинирол и 117 — плацебо. Пациентам, получавшим ротиготин, подбиралась оптимальная доза в течение 4 нед, начиная с 2 мг/24 ч до максимальной — 8 мг/24 ч. У пациентов, получавших ропинирол, максимальная доза достигалась в течение 13 нед и составляла 8 мг/24 ч. Пациенты находились на оптимальной дозе в течение 6 мес. В конце лечения в группе ротиготина оптимальная доза совпадала с максимальной разрешенной — 8 мг/24 ч у 92% пациентов.
Улучшение на 20% наблюдалось у 52% пациентов в группе ротиготина, 68% — в группе ропинирола и 30% — в группе плацебо. Различие между группами ротиготина и плацебо составило 21,7%, между ропиниролом и плацебо — 38,4%, а между ропиниролом и ротиготином — 16,6%. Значение улучшения по УШОБП достигло 6,83 балла в группе ротиготина, 10,78 балла — в группе ропинирола и 2,33 балла — у пациентов, получавших плацебо (все различия были статистически значимыми).
В двух других исследованиях ротиготин назначали пациентам, получавшим сопутствующую терапию препаратами леводопы. Начальная доза ротиготина 4 мг/24 ч каждую неделю повышалась на 2 мг/24 ч до достижения оптимальной. В качестве первичного критерия эффективности использовали продолжительность периода «выключения» (в часах).
В первом из этих двух двойных слепых исследований сравнивали эффективность ротиготина в дозе 8 мг/24 ч (113 пациентов) и 12 мг/24 ч (109 пациентов) и плацебо (119 пациентов). Пациенты находились на оптимальной дозе в течение 6 мес. В конце лечения улучшение на 30% наблюдалось у 57 и 55% пациентов соответственно на фоне получения 8 и 12 мг ротиготина в день и 34% пациентов в группе плацебо. Среднее уменьшение продолжительности периода «выключения» в период лечения ротиготином составило соответственно 2,7 и 2,1 ч, а в группе плацебо — 0,9 ч (различия были статистически значимыми).
Во втором двойном слепом исследовании 201 пациент получал ротиготин, 200 — прамипексол и 100 — плацебо.
В группе ротиготина начальная доза составляла 4 мг/24 ч и увеличивалась до максимальной — 16 мг/24 ч.
В группе прамипексола начальная доза составляла 0,375 мг в день в течение первой недели, 0,75 мг/кг в течение второй недели и в дальнейшем увеличивалась на 0,75 мг в день каждую неделю до максимальной — 4,5 мг в день. В каждой группе пациентов лечение продолжалось в течение 4 мес. В конце лечения улучшение по крайней мере на 30% наблюдалось у 60% пациентов, получавших ротиготин, 67% пациентов, получавших прамипексол, и 35% — в контрольной группе.
Среднее уменьшение продожительности периода «выключения» на фоне лечения ротиготином составило 2,5 ч, прамипексолом — 2,8 ч, плацебо — 0,9 ч (все различия между исследуемыми веществами и плацебо были статистически значимыми).
Фармакокинетика
Всасывание. После накожного применения в виде пластыря трансдермального (ПТ) ротиготин непрерывно высвобождается и абсорбируется через кожу. Css ротиготина достигается через 1–2 дня применения и поддерживается в течение 24 ч в пределах тех же значений при однократном ежедневном применении. В диапазоне доз от 1 до 24 мг/сут наблюдается пропорциональный дозе рост концентрации ротиготина в плазме крови.
Примерно 45% ротиготина высвобождается из ПТ за 24 ч. Абсолютная биодоступность ротиготина при накожном применении в виде ПТ составляет около 37%.
Чередование участков аппликации ПТ может сопровождаться суточными колебаниями концентрации ротиготина в плазме крови. Различия в биодоступности составляют от 2 до 46%, однако клинической значимости это не имеет.
Распределение. Связывание ротиготина с белками плазмы крови in vitro составляет около 92%. Кажущийся Vd — примерно 84 л/кг.
Метаболизм. В организме ротиготин подвергается экстенсивному метаболизму, в основном за счет N-дезалкилирования, а также прямой и опосредованной конъюгации. Данные исследований in vitro показывают, что катализировать N-дезалкилирование ротиготина способны различные изоферменты цитохрома P450. Основные метаболиты биологически неактивны.
Выведение. Примерно 71% активного вещества ротиготина выводится через почки, меньшая часть (около 23%) — с калом.
Клиренс ротиготина при накожном применении составляет около 10 л/мин, а T1/2 — 5–7 ч. Выведение имеет двухфазный характер с первоначальным T1/2 2–3 ч.
Поскольку ротиготин абсорбируется через кожу, влияние приема пищи и состояния ЖКТ на клинические характеристики маловероятно.
Особые группы пациентов
У пациентов с умеренной печеночной недостаточностью и почечной недостаточностью различной степени тяжести значительное повышение концентрации ротиготина в плазме крови не наблюдалось.
При нарушении функции почек повышается концентрация метаболитов ротиготина в плазме крови, но клиническая значимость этого явления неизвестна.
У пациентов с тяжелой печеночной недостаточностью ротиготин не изучался.
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.
Контролируемые исследования ротиготина у беременных не проводились. Результаты доклинических исследований не выявили признаков тератогенной активности, тем не менее определенные дозы оказывали эмбриотоксическое действие. Потенциальный риск эмбриотоксического действия для человека остается неизвестным. Ротиготин не следует применять во время беременности.
Ротиготин снижает секрецию пролактина и уменьшает количество грудного молока. Согласно данным доклинических исследований, ротиготин и/или его метаболиты экскретируются с грудным молоком. В связи с отсутствием данных об экскреции ротиготина с грудным молоком у человека грудное вскармливание следует прекратить.
Женщины детородного возраста. У женщин с сохраненной детородной функцией на фоне лечения ротиготином необходимо использовать адекватную контрацепцию с целью предотвращения беременности.
Фертильность. Влияние ротиготина на репродуктивность исследовали у крыс, кроликов и мышей. Тератогенный эффект ротиготина не был обнаружен у всех трех видов животных, но отмечалась эмбриотоксичность у крыс и мышей в дозах, токсичных для беременных самок.
Ротиготин не влиял на фертильность особей мужского пола у мышей, но отчетливо уменьшал фертильность особей женского пола у крыс и мышей в результате влияния на уровень пролактина, который играет важную роль у грызунов.
Применение
Идиопатическая болезнь Паркинсона — монотерапия ранних стадий без совместного применения с препаратами леводопы или в комбинации с препаратами леводопы (по мере прогрессирования заболевания), в т.ч. на поздних стадиях, на которых терапевтический эффект леводопы становится нестабильным и возникают моторные флуктуации (феномен истощения однократной дозы леводопы, феномен «включения-выключения»).
Категория действия на плод по FDA — C.
Контролируемые исследования ротиготина у беременных не проводились. Результаты доклинических исследований не выявили признаков тератогенной активности, тем не менее определенные дозы оказывали эмбриотоксическое действие. Потенциальный риск эмбриотоксического действия для человека остается неизвестным. Ротиготин не следует применять во время беременности.
Ротиготин снижает секрецию пролактина и уменьшает количество грудного молока. Согласно данным доклинических исследований, ротиготин и/или его метаболиты экскретируются с грудным молоком. В связи с отсутствием данных об экскреции ротиготина с грудным молоком у человека грудное вскармливание следует прекратить.
Женщины детородного возраста. У женщин с сохраненной детородной функцией на фоне лечения ротиготином необходимо использовать адекватную контрацепцию с целью предотвращения беременности.
Фертильность. Влияние ротиготина на репродуктивность исследовали у крыс, кроликов и мышей. Тератогенный эффект ротиготина не был обнаружен у всех трех видов животных, но отмечалась эмбриотоксичность у крыс и мышей в дозах, токсичных для беременных самок.
Ротиготин не влиял на фертильность особей мужского пола у мышей, но отчетливо уменьшал фертильность особей женского пола у крыс и мышей в результате влияния на уровень пролактина, который играет важную роль у грызунов.
Ограничения к применению
Пациенты, принимающие седативные средства, бензодиазепины, антидепрессанты, употребляющие алкоголь (в связи с возможным взаимным усилением эффекта); пациенты с тяжелой печеночной недостаточностью (в связи с возможностью снижения клиренса ротиготина).
Противопоказания
Повышенная чувствительность к ротиготину; проведение МРТ или кардиоверсии во время лечения (см. «Особые указания»); возраст до 18 лет (нет данных по безопасности и эффективности).
Побочные действия
При проведении клинических исследований у пациентов, страдающих болезнью Паркинсона, наиболее часто (более чем у 10% пациентов) наблюдались тошнота, рвота, реакции со стороны кожи в местах наклеивания ПТ, сонливость, головокружение, головная боль.
В начале терапии могут появиться тошнота и рвота легкой и умеренной степени выраженности, эти явления быстро проходят, даже если лечение продолжается.
Ниже представлены сводные данные о побочных реакциях, отмеченных в ходе всех исследований у пациентов с ИБП, в соответствии с общепринятой системно-органной классификацией MedDRA и классификацией ВОЗ по частоте встречаемости: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000); частота не известна (не может быть оценена по имеющимся данным). В каждом диапазоне частот побочные реакции перечислены в порядке уменьшения клинической значимости.
Со стороны иммунной системы: нечасто — повышенная чувствительность, которая может проявляться в виде ангионевротического отека, отека языка и губ.
Нарушения психики: часто — нарушения зрительного и слухового восприятия (включая визуальные и слуховые галлюцинации, зрительные иллюзии), нарушения сна, бессонница, кошмарные сновидения, патологические сновидения, расстройство побуждений, включая патологическое влечение к азартным играм, пандинг — повторные бессмысленные манипуляции с предметами, непреодолимое влечение к покупкам (ониомания); нечасто — приступы повышенной сонливости, внезапный дневной сон, параноидный психоз, нарушения сексуального влечения (гиперсексуальность и повышение либидо), спутанность сознания, дезориентация, ажитация; редко — психотические расстройства, обсессивно-компульсивные расстройства, агрессивное поведение/агрессия, неумеренная потребность в еде, компульсивное переедание, бред, делирий; частота неизвестна — синдром нарушенной регуляции дофамина.
Со стороны нервной системы: очень часто — сонливость, головная боль, головокружение; часто — нарушение сознания (обморок, вазовагальный обморок, потеря сознания), дискинезия, постуральное головокружение, летаргия; редко — судороги, раздражительность.
Со стороны органа зрения: нечасто — нарушение зрительного восприятия, фотопсия (ложное ощущение света в глазах), нарушение остроты зрения.
Со стороны органа слуха и лабиринтные нарушения: часто — вертиго.
Со стороны сердца: часто — ощущение сердцебиения; нечасто — фибрилляция предсердий; редко — наджелудочковая тахикардия.
Со стороны сосудов: часто — постуральная гипотензия, повышение АД; нечасто — снижение АД.
Со стороны дыхательной системы, органов грудной клетки и средостения: часто — икота.
Со стороны ЖКТ: очень часто — тошнота, рвота; часто — запор, сухость во рту, диспепсия; нечасто — боль в животе.
Со стороны кожи и подкожных тканей: часто — эритема, гипергидроз, кожный зуд; нечасто — генерализованный кожный зуд, раздражение кожи, контактный дерматит; редко — генерализованная сыпь.
Со стороны половых органов и молочной железы: нечасто — эректильная дисфункция.
Общие расстройства и нарушения в месте введения: очень часто — реакции в месте аппликации (эритема, зуд, раздражение, чувство жжения, дерматит, папулезная или везикулезная сыпь, изменение цвета кожи, боль, воспаление, экзема, отек, ссадина, крапивница, гиперчувствительность); часто — периферический отек, астеническое состояние (повышенная утомляемость, астения, недомогание).
Данные лабораторных и инструментальных обследований: часто — снижение массы тела, повышение активности КФК; нечасто —повышение активности ферментов печени, в т.ч. AЛT, ACT, ГГТ, повышение массы тела, тахикардия.
Травмы, интоксикации и осложнения манипуляций: часто — падения.
Описание отдельных побочных реакций
В клинических исследованиях при чередовании места аппликации у 35,7% из 830 пациентов с ИБП, применявших ПТ с ротиготином, отмечались местные реакции. В подавляющем большинстве эти реакции были легкой или средней тяжести и ограничены зоной прикрепления ПТ. У 4,3% пациентов местные реакции стали причиной отказа от лечения.
Во время применения ротиготина наблюдалась повышенная сонливость (в т.ч. и днем), включая эпизоды внезапного засыпания. В отдельных случаях эпизоды внезапного засыпания происходили во время вождения автомобиля и приводили к дорожно-транспортным происшествиям.
Расстройства побуждений. При лечении агонистами дофаминовых рецепторов, включая ротиготин, наблюдались патологическое влечение к азартным играм, гиперсексуальность, повышенное половое влечение, компульсивные траты и покупки, компульсивное переедание.
Особые популяции. Повышение уровня КФК выявлено при проведении клинических исследований в Японии (у 3,4% пациентов, получавших ротиготин, и 1,9% пациентов, получавших плацебо). Большинство зарегистрированных случаев было средней степени тяжести и проходило со временем.
Взаимодействие
Поскольку ротиготин относится к группе агонистов дофаминовых рецепторов, возможно снижение его эффективности при одновременном применении с антагонистами дофамина, например нейролептиками (в т.ч. производные фенотиазина, бутирофенон, тиоксантен) или метоклопрамидом. В связи с этим необходимо избегать их совместного применения. В связи с возможным взаимным усилением эффекта ротиготин следует с осторожностью назначать пациентам, принимающим седативные средства, бензодиазепины, антипсихотические средства, антидепрессанты, алкоголь.
Одновременное применение леводопы и карбидопы с ротиготином не оказывает воздействие на фармакокинетику ротиготина, а ротиготин не влияет на фармакокинетику леводопы и карбидопы.
При совместном применении домперидон не влияет на фармакокинетику ротиготина.
Омепразол, ингибитор изофермента CYP2C19, в суточной дозе 40 мг не оказывал влияние на фармакокинетику, в частности метаболизм ротиготина, у здоровых добровольцев при одновременном приеме.
Ротиготин может потенцировать дофаминергический эффект леводопы, вызывать и/или обострять уже существующую дискинезию, что описано и для других агонистов дофаминовых рецепторов.
Совместное применение ротиготина (3 мг/24 ч) и пероральных контрацептивных средств (этинилэстрадиол 0,03 мг, левоноргестрел 0,15 мг) не изменяло фармакокинетику и фармакодинамику последних. Взаимодействие с другими лекарстенными формами гормональных контрацептивных средств не изучено.
Пути введения
Трансдермально.
Меры предосторожности
При недостаточном терапевтическом эффекте ротиготина возможно применение других агонистов дофаминовых рецепторов.
Во избежание ожогов кожи перед проведением МРТ или кардиоверсии ПТ следует удалить.
Ортостатическая гипотензия. Известно, что агонисты дофаминовых рецепторов нарушают системную регуляцию АД, вызывая постуральную/ортостатическую гипотензию. Этот эффект также наблюдался у пациентов, получавших лечение ротиготином, однако при исследовании частота этих явлений была сопоставима с таковой при применении плацебо.
Рекомендуется контролировать АД, особенно в начале лечения, в связи с общим риском развития ортостатической гипотензии, ассоциированной с дофаминергической терапией.
Обмороки. При проведении клинических исследований наблюдались обмороки, но их частота была сопоставима с таковой при приеме плацебо.
Эпизоды дневного засыпания и повышенной сонливости. При применении ротиготина наблюдалась повышенная сонливость и эпизоды внезапного засыпания. Эпизоды внезапного засыпания отмечались и во время дневной активности, в некоторых случаях без каких-либо симптомов-предвестников. Врачи, назначающие ротиготин, на протяжении всего курса терапии должны регулярно оценивать состояние пациентов в отношении повышенной сонливости, т.к. пациенты могут не осознавать наличия данного симптома, пока их напрямую не спросят об этом. При наличии у пациента проявлений повышенной сонливости необходимо решить вопрос о снижении дозы или прекращении терапии.
Злокачественный нейролептический синдром. При резкой отмене ЛС из группы агонистов дофаминовых рецепторов наблюдалось развитие симптомов, напоминающих злокачественный нейролептический синдром. Из этих соображений снижение дозы и отмену терапии рекомендуется проводить постепенно.
Патологическое мышление и поведение. Сообщалось о нарушении мышления и поведения, включая параноидальные идеи, бред, галлюцинации, спутанность сознания, психозоподобное поведение, дезориентацию, возбуждение или агрессивное поведение и делирий.
Фиброзные осложнения. У некоторых больных, получавших агонисты дофаминовых рецепторов из группы алкалоидов спорыньи, отмечались случаи развития легочных инфильтратов, поражения клапанного аппарата сердца, перикардита, плеврального выпота, утолщения плевры, ретроперитонеального фиброза.
Указанные осложнения могут разрешаться при прекращении применения данных средств, однако полное восстановление наблюдается не во всех случаях. Считается, что развитие указанных эффектов связано с эрголиновой структурой производных спорыньи, однако неизвестно, могут ли агонисты дофаминовых рецепторов, не относящиеся к производным спорыньи, вызывать вышеуказанные эффекты.
Нейролептические средства. Пациентам, получающим агонисты дофаминовых рецепторов, не следует назначать нейролептики в качестве противорвотных средств.
Наблюдение у офтальмолога. Рекомендуется регулярное наблюдение у офтальмолога, особенно при появлении расстройств зрения.
Использование тепла. Область применения ПТ с ротиготином не должна подвергаться внешнему воздействию тепла (избыточный солнечный свет, электрические грелки и другие источники тепла, такие как сауна, горячие ванны).
Реакции в месте нанесения. Могут наблюдаться реакции в месте нанесения ротиготина, обычно они бывают слабой и умеренной степени выраженности. Рекомендуется менять место применения каждый день и соблюдать 14-дневный интервал перед повторным нанесением на один и тот же участок кожи.
Если в месте нанесения развились реакции, сохраняющиеся в течение нескольких дней и стойкие, или усилилась выраженность этих реакций, или увеличилась площадь их распространения вне пределов нанесения, необходимо оценить пользу и риск дальнейшего применения ротиготина в виде ПТ для такого пациента. При появлении на фоне лечения ротиготином генерализованной кожной реакции (например аллергическая сыпь — эритематозная, макулезная, папулезная, — или кожный зуд) ротиготин следует отменить.
Дофаминергические побочные реакции. Нужно иметь в виду, что при применении ротиготина в комбинации с леводопой увеличивается частота развития таких дофаминергических побочных реакций, как галлюцинации, дискинезия и периферические отеки.
Периферический отек. В ходе клинических исследований пациентов с болезнью Паркинсона уровень частоты периферических отеков около 4%, отмеченный за 6 мес исследования, оставался неизменным на протяжении всего последующего периода наблюдения в течение 36 мес.
Расстройства побуждений. Необходимо мониторирование с целью выявления расстройств побуждений. Пациенты и лица, ухаживающие за ними, должны быть осведомлены, что поведенческие расстройства, такие как патологическое влечение к азартным играм, повышенное половое влечение, гиперсексуальность, компульсивные траты или покупки, неумеренная постоянная потребность в еде и компульсивное переедание, могут появиться у пациентов, принимающих агонисты дофаминовых рецепторов, в т.ч. ротиготин. При появлении этих симптомов необходимо решить вопрос о снижении дозы или постепенном прекращении приема.
Влияние на способность управлять автомобилем и работать с механизмами. Ротиготин может существенно влиять на способность управлять автомобилем и работать с механизмами.
Пациенты с повышенной сонливостью и/или эпизодами внезапного дневного сна должны быть информированы о том, что им необходимо исключить управление автомобилем и занятия такими видами деятельности, при выполнении которых снижение концентрации внимания может подвергнуть их самих или других людей риску получить серьезную травму или повлечь смерть (например управление производственными механизмами).
Передозировка
Симптомы: наиболее вероятные симптомы передозировки ротиготина являются следствием фармакологического действия агонистов дофаминовых рецепторов и включают тошноту, рвоту, снижение АД, непроизвольные движения, галлюцинации, спутанность сознания, судороги и другие признаки центральной дофаминергической стимуляции.
Лечение: специфический антидот при передозировке ротиготина отсутствует. При подозрении на передозировку необходимо решить вопрос об удалении ПТ с кожи. Концентрация ротиготина в крови начинает снижаться после удаления ПТ. Если необходимо прекратить лечение, отмену ротиготина следует проводить постепенно из-за риска развития злокачественного нейролептического синдрома.
Контроль за состоянием пациента следует осуществлять в условиях стационара, проводя мониторинг сердечного ритма, ЧСС и АД.
В связи с тем, что ротиготин более чем на 90% связывается с белками, польза от гемодиализа сомнительна. Лечение передозировки симптоматическое и предполагает мониторирование и поддержание жизненно важных функций.