Фармакологические группы:
Международный классификатор болезней (МКБ-10):
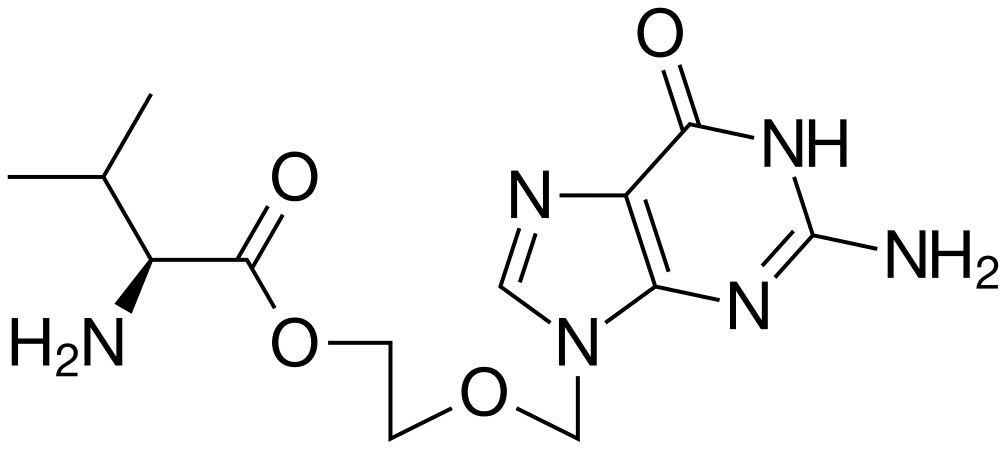
Химическое название
Фармакология
Валацикловир — пролекарство, в организме быстро и почти полностью превращается в ацикловир, который после фосфорилирования приобретает специфическую активность. Ацикловир является структурным аналогом пуриновых нуклеозидов (нормальные компоненты ДНК), взаимодействует с вирусной ДНК-полимеразой и блокирует размножение вирусов. Избирательная противогерпетическая активность обусловлена сродством к тимидинкиназе Herpes simplex, Varicella zoster и вируса Эпштейна-Барр. Под действием тимидинкиназы вирусов трансформируется в ацикловирмонофосфат, при участии гуанилаткиназы клеток человека — в ацикловирдифосфат и затем — в активную форму ацикловиртрифосфат. Трифосфат блокирует репликацию вирусной ДНК за счет конкурентного ингибирования вирусной ДНК-полимеразы и торможения элонгации цепи ДНК. Ацикловир in vitro активен в отношении вирусов Herpes simplex 1 и 2 типа, Varicellа zoster (менее активен, чем в отношении Herpes simplex, вследствие более эффективного фосфорилирования соответствующей тимидинкиназой), вируса Эпштейна-Барр, ЦМВ и человеческого вируса герпеса 6 типа.
Резистентность штаммов Herpes simplex и Varicellа zoster развивается вследствие фенотипического дефицита вирусной тимидинкиназы, либо из-за скрытых изменений в тимидинкиназе или ДНК-полимеразе; устойчивость встречается в исключительных случаях у пациентов с нормальным иммунологическим статусом и значительно чаще на фоне выраженного иммунодефицита (при инфицировании ВИЧ, у больных, получающих химиотерапию по поводу злокачественных новообразований и др.).
Фармакокинетика
После приема внутрь валацикловир быстро абсорбируется из ЖКТ и в результате метаболизма при «первом прохождении» через кишечник и/или печень вследствие ферментативного гидролиза быстро и почти полностью (99%) превращается в ацикловир и L-валин.
Фармакокинетика валацикловира и ацикловира после приема внутрь изучалась в 14 исследованиях на здоровых взрослых добровольцах (n=283).
При приеме валацикловира гидрохлорида в дозе 1000 мг абсолютная биодоступность ацикловира составляет (54,5±9,1)% и не зависит от приема пищи. Фармакокинетические параметры после приема различных доз валацикловира гидрохлорида не пропорциональны дозе. Так, после однократного приема валацикловира гидрохлорида в дозах 100, 250, 500, 750 и 1000 мг Cmах ацикловира достигает 0,83; 2,15; 3,28; 4,17 и 5,65 мкг/мл, AUC — 2,28; 5,76; 11,59; 14,11 и 19,52 ч·мкг/мл соответственно. После многократного приема валацикловира гидрохлорида в дозах 250, 500 и 1000 мг 4 раза в сутки в течение 11 дней Cmах — 2,11; 3,69 и 4,96 мкг/мл и AUC — 5,66; 9,88 и 15,70 ч·мкг/мл соответственно. Tmax составляет 1,6–2,1 ч. Концентрации в плазме неизмененного валацикловира низкие, Cmах ниже 0,5 мкг/мл при всех исследованных дозах, через 3 ч валацикловир уже не определяется в плазме; связывание валацикловира с белками плазмы — 13,5–17,9%. Ацикловир биотрансформируется под действием алкоголь- и альдегиддегидрогеназы и, в меньшей степени, альдегидоксидазы в неактивные метаболиты. Метаболизм валацикловира/ацикловира не связан с ферментами цитохрома P450.
T1/2 валацикловира — менее 30 мин, T1/2 ацикловира после приема валацикловира гидрохлорида составляет 2,5–3,3 ч (у здоровых добровольцев с нормальной функцией почек), у пожилых пациентов (65 лет–83 года) — 3,3–3,7 ч, увеличивается у пациентов с терминальной стадией почечной недостаточности. Валацикловир выводится с мочой (45,6%) и с фекалиями (47,12%) в течение 96 ч. Почечный клиренс — около 255 мл/мин. Из всего количества валацикловира, выводимого почками, более 80–89% элиминируется в виде ацикловира. Менее 1% валацикловира выводится в неизмененном виде. После повторного применения валацикловира у пациентов с нормальной функцией почек ацикловир не кумулирует.
Зависимость параметров фармакокинетики от некоторых факторов
Заболевания печени. У пациентов с заболеваниями печени средней (цирроз, доказанный путем биопсии) или тяжелой (доказанный биопсией цирроз с/без асцита) степени выраженности скорость, но не степень превращения валацикловира в ацикловир, снижается; T1/2 ацикловира не изменяется.
ВИЧ-инфицированные пациенты. У 9 пациентов с ВИЧ (число CD4 клеток <150 клеток/мм3) при приеме валацикловира гидрохлорида в дозе 1000 мг 4 раза в сутки в течение 30 дней фармакокинетические показатели валацикловира и ацикловира не отличались от наблюдаемых у здоровых добровольцев.
Тератогенность. Валацикловир не оказывал тератогенного действия у крыс и кроликов при введении в дозах 400 мг/кг в период органогенеза (при этом концентрации в плазме превышали таковую у человека в 10 и 7 раз соответственно).
Фертильность. Валацикловир не вызывал нарушений фертильности у самцов и самок крыс, получавших внутрь дозу 200 мг/кг/сут (при этом концентрация в крови превышала таковую у человека в 6 раз).
Клинические испытания валацикловира у детей
65 детей в возрасте от 12 до 18 лет принимали таблетированную форму валацикловира внутрь в течение 1-2 дней по поводу герпеса. Частота, характер и интенсивность нежелательных побочных реакций (в т. ч. отклонения лабораторных показателей) были схожи с таковыми в группе взрослых пациентов.
У группы пациентов подросткового возраста, получавших валацикловир в дозе 1-2 г 2 раза в сутки в течение 1 дня (n=65) и у группы плацебо (n=30) были отмечены головная боль (17%, 3%), тошнота (8%, 0%).
Применение при беременности и кормлении грудью
Беременность. Возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода (адекватных и строго контролируемых исследований безопасности применения у беременных женщин не проведено).
Данные об исходе беременности у женщин, принимавших ацикловир системного действия в I триместре беременности (ацикловир является активным метаболитом валацикловира), не показали увеличения числа врожденных пороков у детей по сравнению с общей популяцией. Поскольку в наблюдение было включено небольшое количество женщин, достоверных и определенных выводов о безопасности валацикловира при беременности сделать нельзя.
Категория действия на плод по FDA — B.
Кормление грудью. Ацикловир, основной метаболит валацикловира, экскретируется с грудным молоком. После назначения валацикловира внутрь в дозе 500 мг Cmax ацикловира в грудном молоке в 0,5–2,3 раза (в среднем в 1,4 раза) превышала соответствующие концентрации в крови матери. Отношение AUC ацикловира, находящегося в грудном молоке, к AUC ацикловира в плазме матери составляло 1,4–2,6 (в среднем 2,2). Среднее значение концентрации ацикловира в грудном молоке — 2,24 мкг/мл. При назначении кормящей матери валацикловира в дозе 500 мг 2 раза в день ребенок подвергнется такому же воздействию ацикловира, как при приеме его внутрь в дозе около 0,61 мг/кг/день. Валацикловир в неизмененном виде не определяется в крови и грудном молоке матери или моче ребенка. Валацикловир следует назначать кормящим женщинам с осторожностью, только в случае необходимости.
Дополнительные сведения о применении валацикловира при беременности
Достаточных контролируемых клинических испытаний валацикловира у беременных женщин не проводилось. Опираясь на данные проспективных исследований применения валацикловира на фоне 749 беременностей можно сказать, что соотношение частоты врожденных дефектов развития у детей, подвергшихся воздействию валацикловира во время внутриутробного развития, и у детей в общей популяции одинаково. Валацикловир может применяться при беременности лишь в том случае, когда потенциальная польза для матери превышает потенциальный риск для плода.
Характеристика
Валацикловир представляет собой хлористоводородную соль L-валилового эфира ацикловира. Валацикловира гидрохлорид — белый или почти белый порошок; максимальная растворимость в воде (при 25 °C) — 174 мг/мл; молекулярная масса 360,80.
Применение
Опоясывающий лишай; инфекции кожи и слизистых оболочек, вызванные вирусом простого герпеса (в т.ч. генитальный герпес); профилактика рецидивов заболеваний, вызванных вирусом простого герпеса.
Беременность. Возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода (адекватных и строго контролируемых исследований безопасности применения у беременных женщин не проведено).
Данные об исходе беременности у женщин, принимавших ацикловир системного действия в I триместре беременности (ацикловир является активным метаболитом валацикловира), не показали увеличения числа врожденных пороков у детей по сравнению с общей популяцией. Поскольку в наблюдение было включено небольшое количество женщин, достоверных и определенных выводов о безопасности валацикловира при беременности сделать нельзя.
Категория действия на плод по FDA — B.
Кормление грудью. Ацикловир, основной метаболит валацикловира, экскретируется с грудным молоком. После назначения валацикловира внутрь в дозе 500 мг Cmax ацикловира в грудном молоке в 0,5–2,3 раза (в среднем в 1,4 раза) превышала соответствующие концентрации в крови матери. Отношение AUC ацикловира, находящегося в грудном молоке, к AUC ацикловира в плазме матери составляло 1,4–2,6 (в среднем 2,2). Среднее значение концентрации ацикловира в грудном молоке — 2,24 мкг/мл. При назначении кормящей матери валацикловира в дозе 500 мг 2 раза в день ребенок подвергнется такому же воздействию ацикловира, как при приеме его внутрь в дозе около 0,61 мг/кг/день. Валацикловир в неизмененном виде не определяется в крови и грудном молоке матери или моче ребенка. Валацикловир следует назначать кормящим женщинам с осторожностью, только в случае необходимости.
Дополнительные сведения о применении валацикловира при беременности
Достаточных контролируемых клинических испытаний валацикловира у беременных женщин не проводилось. Опираясь на данные проспективных исследований применения валацикловира на фоне 749 беременностей можно сказать, что соотношение частоты врожденных дефектов развития у детей, подвергшихся воздействию валацикловира во время внутриутробного развития, и у детей в общей популяции одинаково. Валацикловир может применяться при беременности лишь в том случае, когда потенциальная польза для матери превышает потенциальный риск для плода.
Ограничения к применению
Нарушения функции почек, клинически выраженные формы ВИЧ-инфекции, детский возраст до 12 лет (безопасность и эффективность применения не определены).
Противопоказания
Гиперчувствительность (в т.ч. к ацикловиру), трансплантация костного мозга, трансплантация почки (см. «Меры предосторожности»).
Побочные действия
В таблице 1 представлены побочные эффекты, часто наблюдавшиеся при лечении валацикловиром (1 г 3 раза в день) у иммунокомпетентных пациентов с опоясывающим лишаем в период проведения рандомизированных двойных слепых клинических испытаний.
Таблица 1
Побочные явления, наблюдавшиеся при проведении клинических испытаний у пациентов с опоясывающим лишаем
| Побочный эффект | Процент пациентов | |
| Валацикловир (n=967) | Плацебо (n=195) | |
| Тошнота | 15 | 8 |
| Головная боль | 14 | 12 |
| Рвота | 6 | 3 |
| Головокружение | 3 | 2 |
| Абдоминальная боль | 3 | 2 |
В таблице 2 представлены побочные эффекты, наблюдавшиеся при лечении валацикловиром у пациентов с генитальным герпесом в период проведения клинических испытаний.
Таблица 2
Побочные явления, наблюдавшиеся при проведении клинических испытаний у пациентов с генитальным герпесом
| Побочный эффект | Процент пациентов | |||||
| Лечение генитального герпеса | Супрессивная терапия генитального герпеса | |||||
| Валацикловир 1 г 2 раза в день (n=1194) | Валацикловир 500 мг 2 раза в день (n=1159) | Плацебо (n=439) | Валацикловир 1 г 4 раза в день (n=269) | Валацикловир 500 мг 4 раза в день (n=266) | Плацебо (n=134) | |
| Тошнота | 6 | 5 | 8 | 11 | 11 | 8 |
| Головная боль | 16 | 15 | 14 | 35 | 38 | 34 |
| Рвота | 1 | <1 | <1 | 3 | 3 | 2 |
| Головокружение | 3 | 2 | 3 | 4 | 2 | 1 |
| Абдоминальная боль | 2 | 1 | 3 | 11 | 9 | 6 |
| Дисменорея | <1 | <1 | 1 | 8 | 5 | 4 |
| Артралгия | <1 | <1 | <1 | 6 | 5 | 4 |
| Депрессия | 1 | 0 | <1 | 7 | 5 | 5 |
При супрессивной (профилактической, превентивной) терапии для предотвращения рецидивов генитального герпеса у ВИЧ-инфицированных пациентов, принимавших валацикловир в дозе 500 мг 2 раза в день (n=194) и плацебо (n=99), часто отмечались такие побочные эффекты, как головная боль (13 и 8% соответственно), повышенная утомляемость (8/5%), сыпь (8/1%). У пациентов, принимавших валацикловир, отмечались также отклонения лабораторных показателей (в сравнении с плацебо): повышение уровней ЩФ (4/2%), АЛТ (14/10%), АСТ (16/11%), снижение числа нейтрофилов (18/10%) и тромбоцитов (3/0%).
Дополнительные сведения о побочных действиях валацикловира
Клинический опыт применения валацикловира позволил выявить ряд нежелательных явлений, которые не были обнаружены в ходе клинических испытаний. К сожалению, имеющаяся информация не позволяет сделать выводы о частоте развития данных эффектов и указать точную причину их развития.
Приведенные ниже нежелательные явления характеризуются сочетанием следующих свойств: тяжестью, большим количеством сообщений о них, а также высокой вероятностью связи их развития с приемом валацикловира.
Общие расстройства: отек лица, тахикардия, артериальная гипертензия.
Аллергические реакции: анафилактический шок, ангионевротический отек, сыпь, крапивница, кожный зуд, удушье.
Психоневрологические расстройства: атаксия, дизартрия, тремор, кома, энцефалопатия, мания, помрачнение сознания, психозы, слуховые и зрительные галлюцинации.
Расстройства со стороны органов чувств: нарушения зрения.
Гастроинтестинальные расстройства: диарея.
Расстройства со стороны гепато-биллиарного тракта и поджелудочной железы: повышение активности печеночных ферментов в крови, гепатиты.
Расстройства со стороны мочевыделительной системы: почечная недостаточность, боль в области почек (может быть ассоциирована с почечной недостаточностью).
Гематологические расстройства: тромбоцитопения, апластическая анемия, тромботическая тромбоцитопеническая пурпура, гемолитико-уремический синдром.
Кожные проявления: многоформная эритема, сыпь, фотосенсибилизация, аллопеция.
Применение валацикловира при герпесе полости рта
В клинических испытаниях у группы пациентов, получавших валацикловир в дозе 2 г в сутки(n=609) и у группы пациентов, получавших плацебо 1 раз в сутки (n=609) по поводу орального герпеса, были отмечены головная боль (14%, 10%),головокружение (2%, 1%). Частота повышения аланиновой трансаминазы (свыше двух норм) составляла 1,8% в группе пациентов, получавших валацикловир по сравнению с группой плацебо (0,8%).
Другие отклонения лабораторных показателей (уровень гемоглобина, лейкоцитов, креатинина в плазме крови) возникали в обеих группах с одинаковой частотой.
Применение валацикловира с целью снижения риска передачи генитального герпеса
У группы пациентов, получавших валацикловирв дозе 500мг в сутки (n=743), и у группы плацебо (n=741) были отмечены головная боль (29%, 26%), назофарингит (16%, 15%), инфекции верхних дыхательных путей (9%, 10%).
Взаимодействие
Клинически значимых взаимодействий у пациентов с нормальной функцией почек не установлено. Циметидин и пробенецид (по отдельности или вместе) после приема валацикловира в однократной дозе 1000 мг повышают Cmах и AUC и снижают почечный клиренс ацикловира. Фармакокинетика валацикловира не меняется при одновременном приеме с дигоксином, алюминий/магнийсодержащими антацидами, тиазидными диуретиками.
Нефротоксичные препараты повышают риск развития почечной недостаточности и нарушений со стороны ЦНС.
Пути введения
Внутрь (независимо от приема пищи).
Меры предосторожности
С большой осторожностью назначают при любых состояниях, сопровождающихся иммунодефицитом, особенно у ВИЧ-инфицированных пациентов. В период проведения клинических испытаний при приеме валацикловира в высоких дозах (8 г/сут) в течение продолжительного времени регистрировали тромбоцитопеническую пурпуру и/или гемолитический уремический синдром, в редких случаях с летальным исходом, у пациентов с клинически выраженными формами ВИЧ-инфекции, после трансплантации костного мозга или почки (см. «Противопоказания» и «Ограничения к применению»). Не установлены эффективность и безопасность применения валацикловира у иммунокомпрометированных пациентов (за исключением супрессивной терапии генитального герпеса у ВИЧ-инфицированных больных), для супрессивной терапии рецидивирующего генитального герпеса у пациентов с клинически выраженными формами ВИЧ-инфекции (число CD4 клеток <100 клеток/мм3), для лечения генитального герпеса у ВИЧ-инфицированных пациентов, для лечения генерализованного опоясывающего герпеса, для снижения возможности инфицирования генитальным герпесом здорового партнера.
С осторожностью применяют при нарушении функции почек (удлиняется Т1/2 ацикловира), необходима коррекция режима дозирования в зависимости от степени нарушения их функции. У пациентов с заболеваниями почек, получавших высокие дозы валацикловира, наблюдались случаи развития острой почечной недостаточности и нарушений со стороны ЦНС.
Пожилым пациентам во время лечения рекомендуется увеличить объем потребляемой жидкости.
Во время лечения генитального герпеса следует избегать половых контактов (препарат не предохраняет от передачи инфекции).
Риск развития острой почечной недостаточности при приеме валацикловира
Острая почечная недостаточность при приеме валацикловира наблюдалась в следующих случаях:
- У пациентов с заболеваниями почек, которые получали валацикловир в дозах, превышающих рекомендованные для больных со сниженной почечной функцией;
- У пациентов, получавших другие нефротоксические препараты;
- У пациентов с обезвоживанием. Ацикловир может выпадать в осадок в почечных канальцах в случае превышения порога его растворимости (2,5 мг/мл) во внутриканальцевой жидкости. Адекватная гидратация обязательна для всех пациентов, получающих валацикловир.
В случае развития острой почечной недостаточности и анурии, пациентам показан гемодиализ, который следует проводить до восстановления почечной функции.
Дополнительные сведения о побочных действиях валацикловира
При приеме валацикловира как у взрослых пациентов, так и у детей, вне зависимости от функционального состояния почек, наблюдались неблагоприятные реакции со стороны ЦНС: беспокойство, тревога, галлюцинации, делирий, энцефалопатия. У пациентов пожилого возраста побочные эффекты со стороны ЦНС развивались чаще. При возникновении неблагоприятных побочных реакций со стороны ЦНС прием валацикловира следует прекратить.
Передозировка
Симптомы: отложение осадка ацикловира в почечных канальцах.
Лечение: гемодиализ (при острой почечной недостаточности и анурии).